在第六例“治愈”患者出现之前,全球已经有五人被认为实现了艾滋病“治愈”,分别是来自柏林、伦敦、杜塞尔多夫、纽约和加利福尼亚州希望之城的病人。这五人都进行了骨髓移植来治疗严重的癌症病例,接受来自CCR5基因突变捐赠者的干细胞。这种突变可以阻止艾滋病病毒进入人体细胞。

2018年,“日内瓦病人”同样接受了干细胞移植,以治疗一种白血病。但法国和瑞士的研究人员在澳大利亚布里斯班举行的新闻发布会上表示,这一次的移植来自一名没有携带CCR5突变的捐赠者,这意味着病毒仍然能够进入患者的细胞。
然而,研究人员表示,在“日内瓦病人”停止服用抗逆转录病毒治疗20个月后,日内瓦大学医院的医生在他的体内没有发现病毒的痕迹。
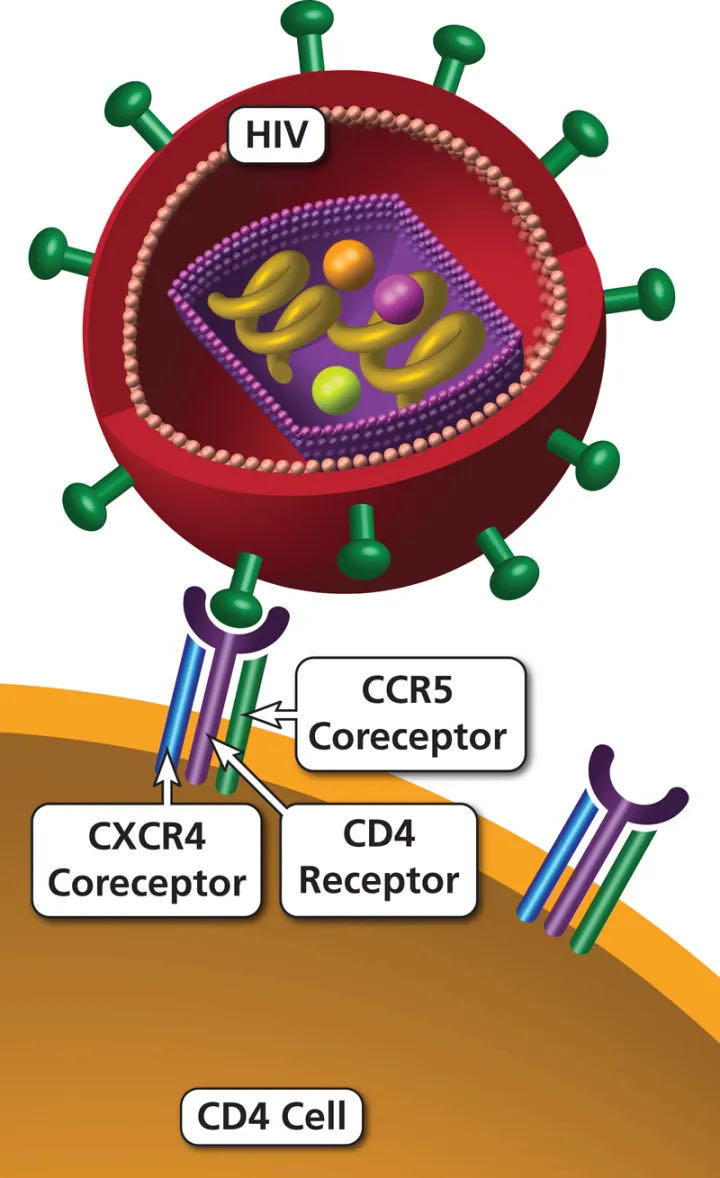
HIV病毒感染人体的原理除了需要通过结合CD4受体进入人体细胞,还需要两个辅助受体,分别是CCR5和CXCR4. 这两个辅助受体只要存在一个,人体细胞即可能感染艾滋病病毒。
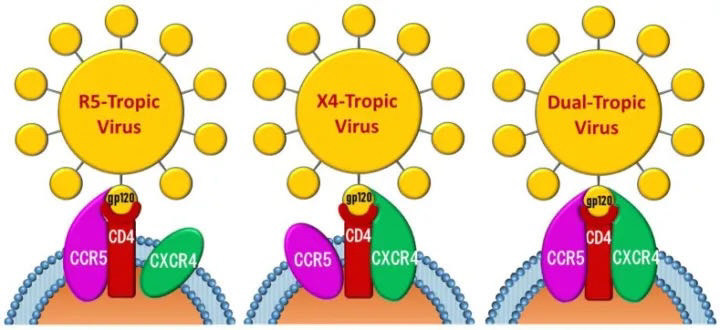
利用何种辅助受体侵入细胞决定HIV病毒株的嗜性。单核细胞/巨噬细胞嗜性的病毒株利用CCR5侵入细胞,称为R5嗜性;T细胞嗜性的病毒株利用趋化CXCR4侵入细胞,称为X4嗜性;而既能利用CCR5,又能利用CXCR4侵入细胞的病毒株称为R5/X4嗜性。
此外,HIV病毒与何种辅助受体结合是随着侵入靶细胞的不同阶段而有所变化的,通常在感染的初期是以CCR5为辅助受体;随着感染程度的加深,病毒由R5嗜性转化为R5/X4嗜性,而双嗜性的HIV病毒是以CXCR4为主要辅助受体的。
所以,原理上同时阻断HIV和CCR5以及CXCR4的结合,即可以阻止HIV感染人体细胞。但由于CXCR4抑制剂尚未被批准上市,所以通过CCR5和CXCR4双抑制剂来阻断艾滋病毒感染人体目前还不可行。
移植骨髓来治疗艾滋病的原理:是通过将带CCR5Δ32基因的干细胞移植到患者体内,干细胞会分化出新的突变型CD4+白细胞,从而重新打造患者的免疫系统,让他们对HIV产生抵抗。但这一方法对病人和供体都有较严格的需求,以及CCR5Δ32基因突变对于人体潜在的危害还不清楚,决定了该方法不可能大规模应用。
关于日内瓦患者在没有移植CCR5Δ32基因的干细胞仍然可以治愈艾滋病,有几个可能的解释:
- 在这种特殊的情况下,移植消除了所有受感染的细胞,而不需要突变;
- 移植后所需的免疫抑制治疗发挥了作用。
尽管目前还无法完全解释其机理,但新的病毒缓解病例是好消息,这样的病例报告在很多方面都将有助于治愈艾滋病。