这个问题可能没有你想象得那么简单哦~
首先回答,两个铁块不能融合是因为表面的存在,实际上,表面物理也是凝聚态物理学中重要的一部分。
对于体材料,其内部必然是稳定的低能态,组成材料的原子或分子通过各种化学键连接起来,从基本相互作用的角度看,这些化学键都是电磁相互作用,像题目中提到的铁,内部的铁原子就是靠金属键连接的。这里还需要注意,电磁相互作用强度与距离呈平方反比,因此随着距离增加,相互作用强度衰减得很快,所以只有距离足够近,才能有足够的吸引力成键。
一个铁块的内部,铁原子必然处于密堆积的状态,至于是那种密堆积方式,我懒得查了【doge】。无论是那种密堆积,对于铁块内部的任一铁原子,其周围都必然有相同数量(应该是12吧)的铁原子对称围绕,这种状态就是铁单质的最低能态,也是最稳定的状态。
但是表面的铁原子不是这样子的,它只有来自体内的方向有铁原子,体外方向没有铁原子。也就是说,对于表面的铁原子,它的对称性出现破缺,表面处原子受到的力或者相互作用与其在晶体内部完全不同。这时它会处于一个高能态。
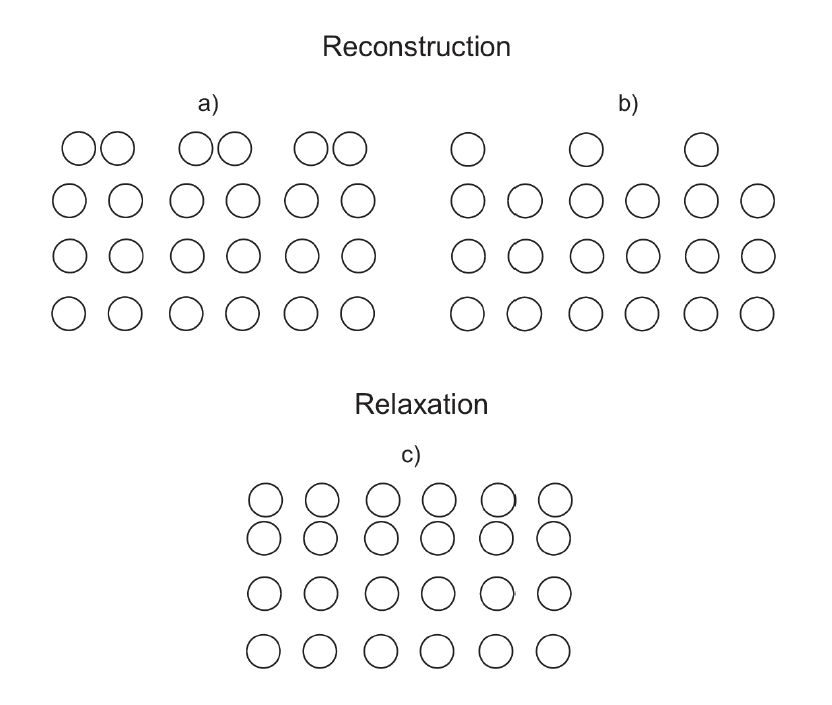
高能态意味着不稳定,因此一般而言,晶体表面会发生重构或弛豫以降低能量,寻求一个更稳定的状态。
对于共价键体系,表面的形成会意味着表面原子确实一部分共价键,这部分共价键由于只有“一半”,我们称它为悬挂键,但悬挂键能量更高,因此有些原子会互相靠近或者缺失一些原子,然后彼此成键以降低能量。这样,表面的布拉维格子就与内部不同了,这就是表面重构。表面重构会使表面态能量降低,但这是相对于悬挂键的情况,相比于体内,表面的能量其实是升高的,这就是表面能的来源。
而对于题目中所说的铁这样的简单金属,其内部的电子分布是非局域性的电子气,因此其成键(金属键)没有方向性。这样的金属表面形成时不会发生重构,而是会发生表面弛豫,表面弛豫即表面的原子在纵向(垂直于表面)的方向会有移动,你可以简单地理解为突出的原子会往里缩,形成一个更平坦的表面。这种弛豫不会改变表面的布拉维格子。
所以你可以看到,表面的融合远远没有你想象得那么简单。
对于一般的共价键体系,由于表面重构,你必须提供足够的能量使表面恢复至悬挂键的状态,然后让两个表面靠得足够近,近到两个表面的自由悬挂键可以相互吸引然后成键,才能使两个表面合二为一。
对于简单金属,则要简单一些,由于金属键没有方向性,我们只需要使两个表面靠的足够近,近到表面的电荷可以相互吸引。就可以做到表面融合。
所以想将两个铁块的融合必须要保证表面足够干净且平坦,干净是为了不影响成键,平坦有助于我们使其足够靠近,必要时可能还需要额外提供一些能量。
需要注意,由于简单金属单质确实比较容易氧化,干净就意味着需要打磨掉表面的氧化层,氧化层的存在会屏蔽内部的铁单质,单质无法顺利地成键。不过若你可以考虑把氧化层融合在一起,但那样需要的能量更高,更困难。当然,干净的含义并不止于此,其他因素,例如杂质、油脂等也有可能影响融合,干净就是排除其他所有因素,保证表面是纯净的铁单质,不过,我认为一些点缺陷(甚至线缺陷)或杂质应该很难避免,也不足以影响融合。另一方面,真空中融合会更容易,因为有气体存在的话,气体容易进入两个表面之间,这样两个表面可能就无法靠的足够近,也就无法融合。